세계 최대 미 바이오시밀러(biosimilar) 시장... K바이오, 38조 시장 도전 Samsung, Celltrion lead biosimilar market in Europe, US
바이오 시밀러 출시 경쟁
세계 최대 의료 시장인 미국에서 올해 특허 기한이 끝났거나 만료를 앞둔 블록버스터(연 매출 1조원 이상 의약품)가 10종을 넘어서면서 새로 열린 연 매출 38조원 ‘바이오 시밀러(biosimilar)’ 시장이 달아오르고 있다. 바이오 시밀러는 특허가 만료된 오리지널 바이오 의약품과 유사하게 만든 복제 의약품을 뜻한다. 국내 바이오 기업들도 특허가 대거 풀린 미국 시장을 겨냥한 바이오 시밀러를 출시하며 경쟁에 뛰어들었다.
Samsung, Celltrion lead biosimilar market in Europe, US
https://www.kedglobal.com/bio-pharma/newsView/ked202503100007
美 38조원 시장 열려
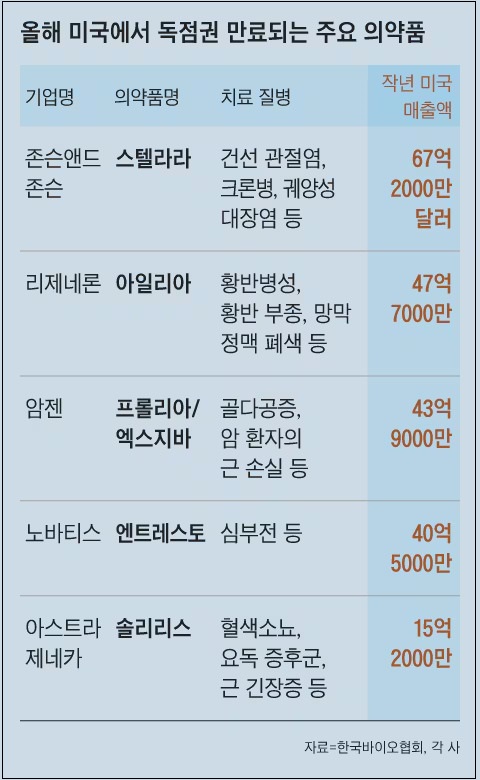
한국바이오협회는 미국의 제약 전문지 피어스파마의 보도를 인용해 올해 미국에서 독점권을 상실했거나 상실을 앞두고 있는 블록버스터 상위 10종의 작년 미국 매출액이 262억달러(약 38조2300억원)에 달한다고 지난 19일 밝혔다. 이 매출액은 각 회사의 실적 발표 자료와 의료 서비스 회사 등의 자료를 분석한 결과다.
이미 특허가 만료된 블록버스터 중 지난해 미국에서 가장 많은 매출을 낸 의약품은 존슨앤드존슨의 자가면역질환 치료제 ‘스텔라라’다. 스텔라라의 지난해 글로벌 매출액은 103억 6000만달러(약 15조1000억원)에 달한다. 이 가운데 67억2000만달러(약 9조8000억원)가 미국 매출액이다. 국내 제약·바이오 상위 10개 기업의 연 매출액을 모두 합쳐도 스텔라라의 연 매출액보다 적다.
이 때문에 많은 제약사가 지난해 스텔라라의 특허 만료를 앞두고 바이오 시밀러를 개발해 왔다. 올해 바이오 시밀러 7종이 미국 시장에서 스텔라라와 경쟁하고 있고, 앞으로 더 많은 스텔라라 바이오 시밀러가 출시될 예정이다.
국내 바이오 기업들도 스텔라라 바이오 시밀러 경쟁에 잇따라 뛰어들었다. 가장 먼저 삼성바이오에피스가 지난달 24일 ‘피즈치바’를 스텔라라 바이오 시밀러로 미국 시장에 출시했다. 셀트리온과 동아에스티는 미 식품의약국(FDA)에서 각각 ‘스테키마’와 ‘이뮬도사’의 품목 허가를 받았고, 올해 중 미국에 출시한다는 계획이다.
삼성바이오에피스와 셀트리온은 골다공증 바이오 시밀러의 미국 출시도 앞두고 있다. 오리지널 의약품은 암젠의 ‘플롤리아’와 ‘엑스게바’로, 골다공증과 골암 치료 등에 사용되고 있다. 플롤리아와 엑스게바의 지난해 세계 매출은 66억달러(약 9조6000억원)로 집계됐다. 이 가운데 미국 매출은 43억9000만달러다.
K 바이오 시밀러, 빠른 임상이 강점
블록버스터의 특허 만료는 바이오 시밀러 개발에 집중해 온 국내 바이오 기업들에 기회다. 오리지널 의약품보다 저렴한 가격에 거의 동일한 효능을 목표로 한 바이오 시밀러는 보험 약가를 절감하고자 하는 도널드 트럼프 행정부의 정책 방향과도 맞는다. 한국바이오협회 바이오경제연구센터에 따르면 FDA가 첫 바이오 시밀러를 허가한 2015년 이래 올해 2월까지 총 68종 바이오 시밀러가 미국 허가를 획득했다. 이 중 20종이 한국산으로, 미국(26 종)에 이어 둘째로 많다.
국내 기업들이 바이오 시밀러 제품군에서 활약하는 것은 임상 결과를 경쟁사 대비 빠르게 얻기 때문인 것으로 분석된다. 미국 임상시험 정보 사이트 클리니컬 트라이얼스에 따르면 바이오 시밀러 개발 과정에서 한국 바이오 기업의 임상 3상 소요 시간이 글로벌 경쟁사에 비해 최대 1년 이상 덜 걸린다.
오리지널 의약품의 화학식을 참고해 동일한 성분으로 제조하면 임상시험 없이 허가를 받을 수 있는 제네릭(복제약)과는 달리 바이오 시밀러는 오리지널 의약품과 동일한 생물학적 특성을 가진다는 임상 근거가 필수적이어서 개발 난도가 높다. 특히 임상 마지막 단계인 임상 3상 과정은 가장 오랜 시간과 비용이 집중되는 구간이다.
이처럼 바이오 시밀러 시장이 급성장하고 있지만, 국내 기업들이 특허 소송에 대비해야 한다는 지적도 나온다. 트럼프 대통령이 지식재산권(IP)을 강조하고 있어 오리지널 의약품을 보유한 제약사들이 권리를 더욱 강하게 주장할 수 있다는 것이다. 일례로 삼성바이오에피스는 블록버스터 ‘아일리아’의 특허를 가진 미국 리제네론 파마슈티컬스와 소송전을 벌이고 있다. 이와 관련해 바이오경제연구센터는 “바이오 시밀러 시장 확대를 위해선 지식재산권을 비롯해 해결해야 할 여러 문제가 있다”고 했다.
* 바이오 시밀러(biosimilar)
특허가 만료된 오리지널 바이오 의약품과 유사하게(similar) 만든 복제 의약품. 바이오 의약품은 살아 있는 생명체로 만들어 오리지널과 100% 똑같은 약을 만들 순 없기 때문에 ‘시밀러’라는 표현을 쓴다. 후발 주자가 쉽게 따라 하기도 어렵다. 반면 화학 합성 의약품을 복제한 의약품은 제너릭(generic)이라고 한다. 화학식만 알면 똑같이 만들 수 있다.
김효인 기자 조선일보
Samsung, Celltrion lead biosimilar market in Europe, US
https://www.kedglobal.com/bio-pharma/newsView/ked202503100007
kcontents








